Cette méthode décrit le prélèvement Actif sur Tube de Florisil ® et l'analyse par chromatographie ionique avec suppression détection conductimétrique de la (des) substance(s) : Acide acétique
Données de validation : Validation complète
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| Acide acétique | 64-19-7 | C2H4O2 |
|
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| Acide acétique | 60,06 | 1,049 | Acide éthanoïque |
Familles de substances
- ACIDES CARBOXYLIQUES ALIPHATIQUES
Principe et informations
Cette méthode doit être utilisée pour les prélèvements d'acide acétique essentiellement sous forme gazeuse. En présence d'un brouillard important, les prélèvements devront être réalisés à l'aide d'une cassette contenant des filtres imprégnés, suivant les préconisations de la méthode M-321.
L'acide acétique est prélevé sur le support de collecte, mis en solution dans l'éluant utilisé et dosé sous forme d'acétate par chromatographie ionique.
Ces essais de validation ont été réalisés pour permettre le dosage de l’acide acétique dans l'air, pour des concentrations allant de 2 mg/m3 (0,1 VLEP-CT à 1 L/min) à 40 mg/m3 (2 VLEP-CT à 1 L/min). Le domaine de validation a été choisi par rapport au projet de recommandation de l’ANSES pour une VLEP-CT de 20 mg/m3 (Rapport en consultation du 30/06/2014 au 02/09/2014).
Cette méthode a été validée en suivant les référentiels normatifs. Toutes les données de validation ainsi que les calculs des performances de la méthode sont indiqués dans les données de validation.
Le 31 janvier 2017 la parution de la directive européenne 2017/164 définie une VLEP-8h à 25 mg/m3 et une VLEP-CT à 50 mg/m3 pour l'acide acétique. La méthode n'a pas été validée pour ces nouvelles valeurs limites.
Principe de prélèvement et d'analyse
-
État physique
Gaz et vapeurs -
Type de prélèvements
Actif -
Nom du dispositif
Tube de Florisil ® -
Plus d'informations
-
Technique analytique
CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION -
Injecteur
PASSEUR AUTOMATIQUE -
Détecteur
CONDUCTIMETRIE
Domaine d'application
| Substance | Quantité minimum sur le dispositif | Quantité maximum sur le dispositif | Concentration minimum | Concentration maximum | Volume maximum |
|---|---|---|---|---|---|
| Acide acétique | 30 µg |
1200 µg |
2 mg/m3 |
80 mg/m3 |
15 L |
Réactifs
- ACIDE SULFURIQUE
- EAU ULTRAPURE
- HYDROXYDE DE SODIUM
- SOLUTION ETALON 1g/L
Méthode de prélèvement
Dispositifs de prélèvement actif pour le prélèvement de gaz ou vapeurs
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
TUBE 50 mm diam 8 mm -
Support ou substrat de collecte
- SILICATE DE MAGNESIUM (FLORISIL®)
-
Quantité de support dans la plage de mesure (mg)
400 -
Quantité de support dans la plage de garde (mg)
200 -
Préparation du substrat
Les deux plages de Florisil® (30-60 mesh) sont maintenues par deux tampons de laine de verre.

Conditions de prélèvement
-
Débit de prélèvement (L/min)
1 -
15 minutes (VLEP-CT possible dans ces conditions)
oui
Pompe de prélèvement
- Pompe à débit de 1 à 3 L/min
Préparation des dispositifs de prélèvement en vue d’une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Durée de conservation prélèvements avant analyse
30 jour(s) -
Conditions de conservation avant analyse
Après les prélèvements, les tubes peuvent être conservés 30 jours à température ambiante sans perte significative.
-
Nombre d'étapes de préparation
1 -
Conditions de conservation échantillon préparé avant analyse
Une fois extrait, les échantillons ne sont pas stables. Les solutions d'extraction doivent être dosées directement après la désorption des tubes.
Une étape de préparation :
Étape de préparation N°1
-
Séparation des plages
oui -
Solvant ou solution
- ELUANT
-
Type de préparation
Désorption -
Volume
20 mL -
Ultrasons
- Temps d'ultrasons : 10 min
-
Autres conditions de préparation
- Transférer séparément chaque plage de Florisil® dans des flacons de désorption.
- Ajouter 20 mL d’éluant pour la plage de 400 mg et 10 mL d'éluant pour la plage de 200 mg.
-
Filtration
Les échantillons sont filtrés sur membrane 0,45 µm avant analyse.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION
-
Injecteur
- PASSEUR AUTOMATIQUE
-
Colonne
- ECHANGEUSE D'IONS
- SUPRESSEUR
-
Détecteur
- CONDUCTIMETRIE
Étalonnage et expression des résultats
La méthode d'étalonnage indiquée est celle utilisée lors du développement. Elle n'a cependant pas de caractère obligatoire
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- ELUANT
-
Commentaires
L'étalonnage doit être réalisé en reconstituant la matrice, donc avec Florisil® (400 mg de Florisil® pour 20 mL).
-
Calcul de la quantité de substance sur le dispositif
Les quantités obtenues sont données en acétate. La concentration atmosphérique en acide acétique est calculée comme suit :
-
Expression des résultats
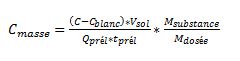
Compléments
Conditions d'analyse utilisées pour la validation de méthode
- Appareil DIONEX avec une précolonne IonPac® AG10 , une colonne IonPac® AS10 et une membrane de suppression ASRS-ultra 4 mm.
- Éluant : 80 mM NaOH, débit : 1 mL/min.
- Régénérant : 25 mM H2SO4, débit : 6 mL/min.
- Volume injecté : 50 µL.
Remarques
- Les conditions chromatographiques ont été optimisées pour obtenir une bonne séparation des fluorures, formates et acétates. L'éluant est à optimiser en fonction du type de colonne choisi et des substances à doser.
- Si la quantité de polluant sur la deuxième plage M2 > 5 % de la première plage M1, le prélèvement est considéré comme non représentatif de l'exposition.
Interférences
Les chlorures d’acides sont hydrolysés en acides carboxyliques et acides hydrochloriques sur les supports de collecte, dans l’air humide, et en solution. Par conséquent, la méthode de prélèvement peut surestimer la concentration en acide carboxylique dans l’air.
Historique
| version | date | Modification(s) faisant l’objet de la nouvelle version | Paragraphes concernés |
|---|---|---|---|
| M-423/V01 | Février 2018 | Création Prélèvement sur tube Florisil d'acide acétique Analyses par chromatographie ionique avec colonne de suppression |
Date de mise à jour : février 2018
