Cette méthode décrit le prélèvement en mode Actif sur cassette et l'analyse par HPLC détection UV de la (des) substance(s) : MHHPA ; HHPA.
Données de validation : Validation complète
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| HHPA | 85-42-7 |
C8H10O3 |
|
| MHHPA | 25550-51-0 |
C9H12O3 |
|
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| HHPA | 154,17 |
Anhydride hexahydrophtalique, Anhydride cyclohexane-1,2-dicarboxylique, Anhydride cyclohexane-1,2-dicarboxylique |
||
| MHHPA | 168,2 |
Anhydride méthylhexahydrophtalique, Anhydride hexahydrométhylphtalique |
Familles de substances
- ANHYDRIDES
Principe et informations
La détermination des concentrations en anhydrides d'acide dans les atmosphères de travail est réalisée par prélèvement de l’air à l’aide d’une cassette porte-filtre fermée, en polypropylène opaque (ou polypropylène blanc, résistant aux solvants), contenant un filtre- ou membrane- tampon puis un filtre en fibre de quartz de diamètre 37 mm, imprégné d’un réactif de dérivation. Ce réactif, la 1-(2-méthoxyphényl) pipérazine, réagit avec les anhydrides présents sur le support de collecte pour former des amides selon le schéma suivant :
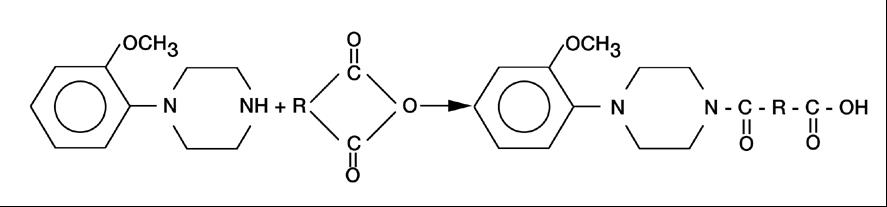
Les dérivés retenus sur le dispositif sont ensuite désorbés par l’acétonitrile et analysés par chromatographie en phase liquide avec détection UV.
Principe de prélèvement et d'analyse
-
État physique
Aérosols (mélange de gaz ou vapeurs / particules) -
Type de prélèvements
Actif -
Nom du dispositif
cassette -
Plus d'informations
-
Technique analytique
CHROMATOGRAPHIE EN PHASE LIQUIDE -
Injecteur
PASSEUR AUTOMATIQUE -
Détecteur
ULTRAVIOLET (UV)
Domaine d'application
| Substance | Quantité minimum sur le dispositif | Quantité maximum sur le dispositif | Concentration minimum | Concentration maximum | Volume maximum |
|---|---|---|---|---|---|
| HHPA | 20 µg |
400 µg |
|||
| MHHPA | 20 µg |
400 µg |
Réactifs
- 1-(2-METHOXYPHENYL)PIPERAZINE
- ACETONITRILE
- EAU
- HYDROGENOPHOSPHATE DE POTASSIUM
- TETRAHYDROFURANE
Méthode de prélèvement
Utilisation de la cassette fermée pour le prélèvement d’aérosols
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
CASSETTE POLYPROPYLENE 37 mm 2 pièces -
Support ou substrat de collecte
- FILTRE FIBRE DE QUARTZ IMPREGNE
-
Préparation du substrat
Préparation de la solution d’imprégnation (réactif de dérivation) :
Préparer une solution à 3 g/L de méthoxyphényl pipérazine dans le tétrahydrofurane (THF).
Imprégnation des filtres :
Imprégner les filtres par trempage et agitation du filtre dans une quantité suffisante (pour les recouvrir) de solution réactive de mpp/THF. Les laisser sécher à l’air libre jusqu’à évaporation totale du solvant.
Conservation des filtres imprégnés:
Utiliser les filtres dans les 3 semaines qui suivent leur imprégnation.
-
Commentaires, conseils et consignes
Cassette porte-filtre fermée, en polypropylène opaque ou propylène blanc (résistant aux solvants) contenant un filtre en fibre de quartz de diamètre 37 mm imprégné, posé au-dessus d'un filtre-tampon.
Tester l’étanchéité du dispositif de prélèvement.
http://www.inrs.fr/dms/inrs/PDF/metropol-intervention-preparation.pdf
La pureté du réactif (mpp) et la conservation dans le temps de la solution d’imprégnation peuvent influer sur la qualité des blancs-filtres et sur la limite de quantification LQa.
Conditions de prélèvement
-
Débit de prélèvement (L/min)
1 -
Temps de prélèvement maximum en heures
8
Pompe de prélèvement
- Pompe à débit de 0,1 à 3,5 L/min
Conditionnement particulier
-
Description
Refermer hermétiquement les cassettes et les placer, dans les 24 heures, à -20°C.
Compléments
Un blanc de terrain au moins est réalisé pour chaque série de prélèvements, la cassette étant alors ouverte sur le lieu de prélèvement au début de la série et refermée immédiatement avec le même type de bouchons que les cassettes de prélèvement.
Préparation des dispositifs de prélèvement en vue d'une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Nombre d'étapes de préparation
1 -
Commentaires sur les étapes
Le protocole d’analyse décrit ci-après permet de prendre en compte un éventuel dépôt de la (des) substance(s) sur les parois de la cassette.
La désorption du (des) dérivé(s) retenu(s) sur le dispositif est effectuée à l'aide des ultra-sons.
-
Durée de conservation échantillon préparé avant analyse
8 jour(s) -
Conditions de conservation échantillon préparé avant analyse
Effectuer l'analyse des échantillons désorbés (échantillons prélevés et étalons) dans les 8 jours.
Une étape de préparation :
Étape de préparation N°1
-
Solvant ou solution
- ACETONITRILE
-
Type de préparation
Désorption -
Volume
6 mL -
Ultrasons
- Temps d'ultrasons : 15 min
-
Filtration
Sur filtre 0,45 µm, 25 mm, en polyamide.
-
Commentaires
Placer le filtre dans un flacon à vis étanche et désorber par 5 mL d'acétonitrile. Rincer les parois de la cassette avec 1 mL à rajouter dans le flacon contenant le filtre imprégné.
Passage aux ultra-sons pendant 15 min puis filtration sur filtre 0,45 µm lors du transfert dans le vial d'injection.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- CHROMATOGRAPHIE EN PHASE LIQUIDE
-
Injecteur
- PASSEUR AUTOMATIQUE
-
Colonne
- PHASE INVERSE C18
-
Détecteur
- ULTRAVIOLET (UV)
-
Phase mobile
- ACETONITRILE
- EAU TAMPONNEE
Étalonnage et expression des résultats
La technique d'étalonnage utilisée lors du développement de la méthode revêt un caractère obligatoire pour atteindre le niveau de performances indiqué (sensibilité, rendements, précision).
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- ACETONITRILE
-
Commentaires
L’étalonnage est réalisé par reconstitution de matrice.
Le conditionnement des dispositifs à prévoir pour la préparation des étalons, doit être identique à celui des dispositifs utilisés pour les prélèvements (intégrant la conservation entre prélèvement et analyses).
Les étalons sont :
- préparés à partir de la (des) substance(s) de référence (par exemple, mélange d'isomères disponible commercialement), la préparation comprenant la mise en solution, le dépôt et la dérivation sur les filtres imprégnés préalablement conditionnés - voir ci-dessus-,
- désorbés selon le même protocole que les échantillons prélevés.
La droite d'étalonnage est établie à partir de l'aire totale des pics repérés pour l'anhydride dosé.
Des données complémentaires sont fournies dans le document Données de validation.
-
Calcul de la quantité de substance sur le dispositif
Reporter sur la droite d'étalonnage l'aire totale des pics repérés pour l'anhydride dosé.
L’aire moyenne obtenue pour les blancs-filtres peut être systématiquement soustraite de l’aire des pics étalons et échantillons.
En déduire la concentration en anhydride dans les désorbats (Ci en µg/mL).
Quantité d'anhydride (Mp) sur le dispositif de prélèvement = Mp (µg) = (Ci x Vi)
Ci (µg/mL) = concentration en anhydride dans le désorbat
Vi (mL) = volume du solvant de désorption.
Historique
| Version | Date | Modification(s) faisant l'objet de la nouvelle version |
|---|---|---|
| M-419/V01 | 03/2017 | Création |
Date de mise à jour : mars 2017
