Cette méthode décrit le prélèvement Actif sur cassette avec filtres imprégnés et l'analyse par chromatographie ionique avec suppression détection conductimétrique de la (des) substance(s) : Dioxyde de chlore
Données de validation : Validation partielle
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| Dioxyde de chlore | 10049-04-4 | ClO2 |
|
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| Dioxyde de chlore | 67,45 |
Principe et informations
Dans les conditions de terrain, une grande partie du dioxyde de chlore est dissoute dans l'eau présente sous forme d'aérosol. C'est pourquoi la méthode prélève à la fois le gaz et la fraction aérosol.
Principe de prélèvement et d'analyse
-
État physique
Aérosols (mélange de gaz ou vapeurs / particules) -
Type de prélèvements
Actif -
Nom du dispositif
cassette avec filtres imprégnés -
Plus d'informations
-
Technique analytique
CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION -
Injecteur
PASSEUR AUTOMATIQUE -
Détecteur
CONDUCTIMETRIE
Réactifs
- ACETONE
- CHLORITE DE SODIUM
- EAU
- TRIETHANOLAMINE
Méthode de prélèvement
Utilisation de la cassette fermée pour le prélèvement d’aérosols
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
CASSETTE 37 mm 3 pièces -
Support ou substrat de collecte
- FILTRE FIBRE DE QUARTZ IMPREGNE
- MEMBRANE inf 1 µm
-
Préparation du substrat
Solution d'imprégnation des filtres en fibre de quartz : 25 g de triéthanolamine dans 25 mL d'acétone complétés à 100 mL d'eau déionisée. Déposer sur les filtres 500 µL de solution, faire sécher à 50 °C à l'étuve pendant 1 heure.
La membrane de porosité <1 µM peut être une membrane Teflon ou PVC ou Acrylonitrile.
-
Commentaires, conseils et consignes
Déposer à l'aide d'une pince le filtre en fibre de quartz imprégné au fond de la cassette, puis la membrane
de porosité < 1 µM sur le niveau intermédiaire.
Conditions de prélèvement
-
Débit de prélèvement (L/min)
1 -
15 minutes (VLEP-CT possible dans ces conditions)
oui -
Temps de prélèvement maximum en heures
8
Pompe de prélèvement
- Pompe à débit de 1 à 3 L/min
Conditionnement particulier
-
Choix conditionnement particulier
désorption immédiate
Compléments
Voir également dans les données de validation - compléments, les prélèvements de ClO2 en présence d’autres dérivés chlorés.
Préparation des dispositifs de prélèvement en vue d’une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Durée de conservation prélèvements avant analyse
1 mois -
Conditions de conservation avant analyse
Les filtres imprégnés doivent être désorbés immédiatement après prélèvement.
-
Séparation des plages
oui -
Durée de conservation échantillon préparé avant analyse
1 mois
Une étape de préparation :
Étape de préparation N°1
-
Solvant ou solution
- EAU
-
Type de préparation
Solubilisation -
Volume
10 mL -
Ultrasons
- Temps d'ultrasons : 5 min
-
Autres conditions de préparation
- Après les prélèvements, placer les filtres en fibre de quartz dans des flacons de désorption avec 5 à 20 mL d’eau ultra-pure.
- Ces solutions sont stables un mois à température ambiante (cf. données de validation - compléments).
- Avant l’analyse, soumettre les flacons de désorption à une agitation aux ultrasons pendant 5 à 10 minutes.
- Les solutions obtenues seront filtrées avant injection dans le système chromatographique.
Remarque
Traiter les blancs de terrain et les blancs de laboratoire de la même façon.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION
-
Injecteur
- PASSEUR AUTOMATIQUE
-
Colonne
- ECHANGEUSE D'IONS
- SUPRESSEUR
-
Détecteur
- CONDUCTIMETRIE
Étalonnage et expression des résultats
La méthode d'étalonnage indiquée est celle utilisée lors du développement. Elle n'a cependant pas de caractère obligatoire
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- Même solvant que celui des échantillons
-
Commentaires
Réaliser des étalons à partir de substances de référence, commerciales ou synthétisées en laboratoire. Le solvant utilisé pour réaliser les solutions sera celui choisi pour le traitement des échantillons.
Préparer une gamme d'étalonnage, dans la même matrice que les échantillons (ne pas oublier le filtre imprégné)
-
Calcul de la quantité de substance sur le dispositif
La concentration réelle C (en mg/m3) dans l’air est donnée par :
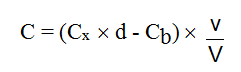
avec :
Cx (mg/L) : concentration de la substance dans l'échantillon
d : facteur de dilution
Cb ( mg/L) : concentration moyenne de la substance dans les blancs de laboratoire
v (mL) : volume de jaugeage
V (L) : volume d’air prélevé
Compléments
Phase mobile à déterminer en fonction de la colonne utilisée. Des exemples sont donnés dans les données de validation - compléments.
Bibliographie
- V. OURY, A. PELTIER. - Prélèvement et dosage du dioxyde de chlore par piégeage spécifique. Mise au point d'une méthode applicable aux ambiances de travail. Cahiers de notes documentaires, 1998, 172, ND 2081, pp. 233-242.
- M.A. WILLEY, C.S. Mc CAMMON. - A solid sorbent personnal sampling method for the simultaneous collection of nitrogen dioxide and nitric oxide in air. American Industrial Hygienist Association Journal, 1997, 38, pp. 358-363.
- D.V. VINJAMOORI, C. S.LING. - Personal monitoring method for nitrogen dioxide and sulfur dioxide with solid sorbent sampling and ion chromatographic determination. Analytical Chemistry, 1981, 53, pp. 1689-1691.
- J.E. SICKLES, P.M. GROHSE, L.L. HODSON. - Development of a method for the sampling and analysis of sulfur dioxide and nitrogen dioxide from ambient air. Analytical Chemistry, 1990, 62, pp. 338-346.
- M. HÉRY, G. HECHT, J.M. GERBER. - Exposure to chloramines in the atmosphere of indoor swimming pools. Annals of Occupational Hygiene, 1995, vol. 39, n° 4, pp.427-439.
Historique
| Version | Date | Modification(s) faisant l’objet | Paragraphes |
|---|---|---|---|
| 033 | Jusqu’au | Création + mises à jour |
|
| 033/V01 | 25/01/2006 | Nouvelle présentation | Réactifs |
| M207/V01 | Novembre 2015 | Mise en ligne Substance unique Prélèvement sur cassette Analyse par chromatographie ionique/conductimétrie |
|
Date de mise à jour : novembre 2015
Ancien numéro de fiche MétroPol : 033
