Cette méthode décrit le prélèvement Actif sur cassette avec filtres imprégnés et l'analyse par spectrophotométrie de la (des) substance(s) : Sulfure d'hydrogène
Données de validation : Validation partielle
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| Sulfure d'hydrogène | 7783-06-4 | H2S |
|
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| Sulfure d'hydrogène | 34,08 | Hydrogène sulfuré |
Principe et informations
L'hydrogène sulfuré est très toxique par inhalation, dangereux pour l'environnement et extrêmement inflammable, sa manipulation doit être faite avec un maximum de précautions.
La détermination de l'hydrogène sulfuré dans les atmosphères de travail est réalisée par prélèvement sur un support de collecte imprégné d'acétate de cadmium transformant l'hydrogène sulfuré en sulfure de cadmium selon la réaction :
Cd(CH3COO)2 + H2S → CdS + 2 CH3COOH
La désorption du support de collecte avec le dichlorhydrate de N,N-diméthyl-1,4-phénylènediamine, en milieu acide, en présence de chlorure ferrique conduit à la formation de bleu de méthylène dont l'intensité de la coloration est déterminée par spectrophotométrie.
Principe de prélèvement et d'analyse
-
État physique
Gaz et vapeurs -
Type de prélèvements
Actif -
Nom du dispositif
cassette avec filtres imprégnés -
Plus d'informations
-
Technique analytique
SPECTROPHOTOMETRIE
Réactifs
- ACETATE DE CADMIUM
- ACIDE CHLORHYDRIQUE
- ACIDE SULFURIQUE
- CHLORURE FERRIQUE
- DICHLORHYDRATE DE N,N-DIMETHYL-1-4-PHENYLENEDIAMINE
- EAU
- EMPOIS D'AMIDON
- GLYCEROL
- SOLUTION d'IODE
- SOLUTION THIOSULFATE DE SODIUM
- SULFURE DE SODIUM
Méthode de prélèvement
Utilisation de la cassette fermée pour le prélèvement d’aérosols
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
CASSETTE 37 mm 4 pièces -
Support ou substrat de collecte
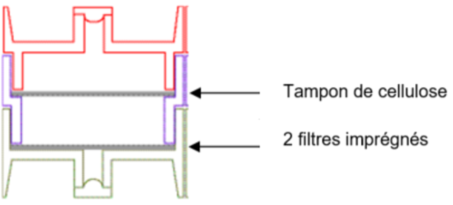
- 2 FILTRES EN FIBRE DE QUARTZ IMPREGNES
- TAMPON EN CELLULOSE
-
Préparation du substrat
La solution d'imprégnation des filtres en fibres en fibre de quartz est faite à l'aide de 1 g d'acétate de cadmium, auquel on ajoute 5 mL de glycérol puis 100 mL d'eau. Déposer 500 µL de cette solution sur les filtres, les faire sécher à l'étuve entre 50°C et 70°C pendant 3 heures.
-
Commentaires, conseils et consignes
Placer les deux filtres imprégnés au fond de la cassette puis un tampon de cellulose sur la deuxième pièce. Fermer ensuite la cassette. Le tampon sera impérativement humidifié par 250 µL d'eau juste avant prélèvement
Conditions de prélèvement
-
Débit de prélèvement mini (L/min)
0,050 -
Débit de prélèvement maxi (L/min)
1 -
15 minutes (VLEP-CT possible dans ces conditions)
oui -
Temps de prélèvement maximum en heures
8 -
Particularités, commentaires, conseils
Pour la comparaison à VLEP-8h, le débit est compris entre 0,05 L/min et 0,2 L/min; pour une comparaison à VLEP-CT le débit est compris entre 0,1 L/min et 1 L/min.
Pompes de prélèvement
- Pompe à débit de 0,02 à 0,5 L/min
- Pompe à débit de 0,1 à 3,5 L/min
Conditionnement particulier
-
Choix conditionnement particulier
stabilisation -
Description
Tenir les échantillons à l'abri de la lumière pendant et après le prélèvement (par exemple en emballant les cassettes dans une feuille d'aluminium).
Compléments
Voir le tableau débits préconisés en fonction de la durée du prélèvement et des comparaisons recherchées dans les données de validation - compléments.
La capacité de piégeage des filtres imprégnés est fortement dépendante de l'hygrométrie, c'est pour cette raison que l'on ajoute un tampon de cellulose en amont des filtres imprégnés mouillé avec 250 µL d’eau ultra-pure juste avant le prélèvement.
Préparation des dispositifs de prélèvement en vue d’une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Conditions de conservation avant analyse
Tenir les échantillons à l'abri de la lumière pendant et après le prélèvement (par exemple en emballant les cassettes dans une feuille d'aluminium).
-
Nombre d'étapes de préparation
1 -
Durée de conservation échantillon préparé avant analyse
24 jour(s)
Une étape de préparation :
Étape de préparation N°1
-
Solvant ou solution
- ACIDE SULFURIQUE
- DICHLORHYDRATE DE N,N-DIMETHYL-1.4-PHENYLENEDIAMINE
- EAU
-
Type de préparation
Percolation -
Volume
250 mL -
Autres conditions de préparation
Préparation des solutions de désorption
Les solutions servant à la désorption sont préparées comme suit :
- Solution d'amine test :
- préparer d'abord une solution mère : ajouter lentement 50 mL d'acide sulfurique concentré à 30 mL d’eau ultra-pure, refroidir puis dissoudre 12 g de dichlorhydrate de N,N- diméthyl-1,4 -phénylènediamine. Cette solution conservée au réfrigérateur est stable indéfiniment.
- Diluer 25 mL de solution mère dans 1 L d'acide sulfurique au demi.
- Solution de chlorure ferrique :
- dissoudre 100 g de chlorure ferrique dans 60 mL d’eau ultra-pure, jauger à 100 mL.
Désorption
montage figure 1
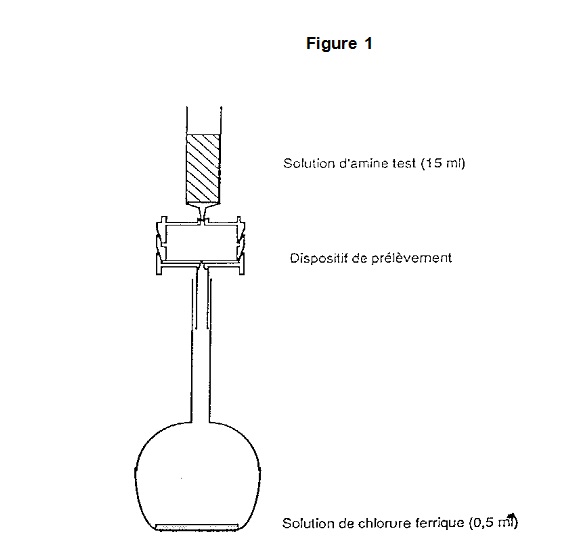
- Dans une fiole jaugée de 250 mL, on introduit 0,5 mL de solution de chlorure ferrique puis 50 mL d’eau ultra-pure.
- Le tampon de cellulose est retiré de la cassette, celle-ci est ensuite placée au-dessus de la fiole jaugée.
- On fait percoler 15 mL de solution d'amine test à travers les filtres.
- Effectuer ensuite 2 rinçages à l’eau ultra-pure.Après 20 minutes (temps nécessaire au développement de la coloration) la solution est amenée au volume avec de l’eau ultra-pure, puis analysée par spectrométrie d'absorption moléculaire dans le visible à 670 nm en cuve de 1 cm.
Remarque
Traiter les blancs (de terrain, de laboratoire) de la même façon.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- SPECTROPHOTOMETRIE
-
Commentaires, conseils ou condition particulières
Colorimétrie avec ʎ = 670 nm
Étalonnage et expression des résultats
La méthode d'étalonnage indiquée est celle utilisée lors du développement. Elle n'a cependant pas de caractère obligatoire
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- Même solvant que celui des échantillons
-
Commentaires
- Préparer une solution de teneur en H2S de l'ordre de 2 g/L, dans une fiole de 100 mL, par dissolution de 1,4 g de Na2S, 9H2O dans de Contrôler le titre de la solution selon la procédure décrite dans les données complémentaires.
- Préparer ensuite une solution à 40 mg/L en H2S par dilution de la solution à 2 g/L.
- La gamme d'étalons est réalisée à partir de cette solution, comme suit :
- mettre respectivement 0 - 1 - 2 - 3 et 4 mL de la solution de Na2S dans des fioles de 250 mL,
- ajouter 15 mL de solution d'amine test et 50 mL d'eau ultra-pure,
- agiter la solution,
- ajouter ensuite 0,5 mL de chlorure ferrique et laisser la coloration se développer pendant
20 minutes,- enfin, jauger la fiole à 250 mL avec de l’eau ultra-pure et effectuer le dosage.
Remarques
- Correspondance entre quantité de Na2S et quantité d'H2S : 1,4 g de Na2S à 35% contiennent 0,49 g de Na2S pur, ce qui correspond à une masse d'environ 0,2 g de H2S.
- Des essais réalisés en dynamique, par génération d'une atmosphère étalon à partir d'H2S gazeux, ont montré que la pente des droites d'étalonnage (densité optique = f (quantité H2S exprimée en µg)), est identique à celle obtenue à partir d’une solution de sulfure de sodium.
- Analyser les solutions étalons et tracer la droite d'étalonnage (la réponse spectrophotométrique de la coloration bleue formée est linéaire à 670 nm jusqu'à une densité optique de 0,6, ce qui correspond à une teneur de 170 à 200 µg d'H2S par échantillon).
- Analyser ensuite les solutions de désorption des échantillons ainsi que les solutions de désorption des filtres servant de blancs (de terrain et de laboratoire).
Bibliographie
- R. VINCENT, J.C. LIMASSET, G. HECHT, J.M. GERBER, A. CICOLELLA. - Détermination simultanée des sulfures de carbones et d'hydrogène dans les atmosphères de travail. Analusis, 1985, V13, n° 9, pp. 415-419.
- Réactions chimiques dangereuses. Paris, INRS, ED 697, 2003, 404 p.
Historique
| Version | Date | Modification(s) faisant l’objet | Paragraphes |
|---|---|---|---|
| 014 | Jusqu'au | Création et mises à jour |
|
| 014/V01.01 | 25/09/2012 | Révision de la terminologie (VLEP-8h, VLCT, Dispositif de prélèvement et support de collecte, eau ultra-pure, blanc de terrain et blanc de laboratoire) | Toute la fiche |
| M-184 | Novembre 2015 | Mise en ligne Prélèvement sur cassette Analyse par spectrophotométrie | |
| M-184 V01 | Juillet 2023 | Correction erreur sur le disposif de prélèvement | Dispositif de prélèvement |
Date de mise à jour : juillet 2023
Ancien numéro de fiche MétroPol : 014
