Cette méthode décrit le prélèvement Actif sur cassette avec filtres imprégnés et l'analyse par chromatographie ionique avec suppression détection conductimétrique de la (des) substance(s) : Ammoniac et sels d'ammonium
Données de validation : Validation complète
Substances
Informations générales
Propriétés physico-chimiques
| Nom | N° CAS | Formule chimique | Classification CMR |
|---|---|---|---|
| Ammoniac, anhydre | 7664-41-7 | NH3 |
|
Plus d'informations
| Nom | Masse molaire | Densité | Synonymes | Fiche toxicologique |
|---|---|---|---|---|
| Ammoniac, anhydre | 17,04 | 0,59 | NH3 |
Principe et informations
L'acide sulfurique, choisi comme solution d’imprégnation, réagit avec le gaz ammoniac selon l’équation :
2NH3 + H2SO4 → (NH4)2SO4
pour former un sel d’ammonium stable et soluble dans l’eau (760 g/L à 20°C) qui peut être dosé par chromatographie ionique.
Principe de prélèvement et d'analyse
-
État physique
Aérosols (mélange de gaz ou vapeurs / particules) -
Type de prélèvements
Actif -
Nom du dispositif
cassette avec filtres imprégnés -
Plus d'informations
-
Technique analytique
CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION -
Injecteur
PASSEUR AUTOMATIQUE -
Détecteur
CONDUCTIMETRIE
Domaine d'application
| Substance | Quantité minimum sur le dispositif | Quantité maximum sur le dispositif | Concentration minimum | Concentration maximum | Volume maximum |
|---|---|---|---|---|---|
| Ammoniac, anhydre | 3,36 µg |
7,46 mg |
0,112 mg/m3 |
249 mg/m3 |
480 L |
Réactifs
- ACIDE SULFURIQUE
- EAU
- SOLUTION ETALON 1g/L
Méthode de prélèvement
Utilisation de la cassette fermée pour le prélèvement d’aérosols
Un dispositif de prélèvement :
Dispositif N°1
-
Type dispositif
CASSETTE 37 mm 3 pièces -
Support ou substrat de collecte
- FILTRE FIBRE DE QUARTZ IMPREGNE
- MEMBRANE inf 1 µm
-
Préparation du substrat
Filtres imprégnés : Déposer sur les filtres en fibres de quartz 500 µL d'une solution d'acide sulfurique à 1,5 M. Faire sécher à l'étuve à 50°C pendant 3 heures.
Bien respecter les conditions d'imprégnation pour éviter un colmatage rapide du filtre.
-
Commentaires, conseils et consignes
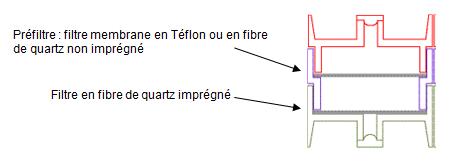
Déposer au fond de la cassette un filtre imprégné et sur la pièce intermédiaire une membrane de porosité inférieure à 1µm (fibre de quartz ou membrane Teflon) non imprégné avec une pince puis refermer la cassette.
Conditions de prélèvement
-
Débit de prélèvement mini (L/min)
1 -
Débit de prélèvement maxi (L/min)
2 -
Débit de prélèvement (L/min)
2 -
15 minutes (VLEP-CT possible dans ces conditions)
oui -
Temps de prélèvement maximum en heures
8 -
Particularités, commentaires, conseils
Les prélèvements peuvent être réalisés à 1 L/min pendant 8 h ou 2 L/min pendant maximum 4 h.
Pour les fortes expositions, il est recommandé de réaliser les prélèvements à 1 L/min. (voir données de validation - essai de claquage)
Pompe de prélèvement
- Pompe à débit de 1 à 3 L/min
Préparation des dispositifs de prélèvement en vue d’une intervention en entreprise
Méthode d'analyse
Principe général de l'analyse en laboratoire
Préparation d'analyse
-
Durée de conservation prélèvements avant analyse
2 mois -
Séparation des plages
oui -
Nombre d'étapes de préparation
3 -
Commentaires sur les étapes
La première étape concerne la désorption du filtre imprégné.
La seconde étape concerne la désorption du préfiltre.
La troisième étape consiste à récupérer la substance sur les parois de la cassette.
3 étapes de préparation :
Étape de préparation N°1
-
Solvant ou solution
- EAU
-
Type de préparation
Désorption -
Volume
20 mL -
Ultrasons
- Temps d'ultrasons : 5 min
-
Filtration
Filtrer les solutions avant analyses
Étape de préparation N°2
-
Solvant ou solution
- SOLUTION BLANC FILTRE
-
Type de préparation
Désorption -
Volume
5 mL -
Ultrasons
- Temps d'ultrasons : 5 min
-
Autres conditions de préparation
Préparer un volume de blanc filtre en plaçant n filtres imprégnés vierges dans n x 20 mL d'eau.
Désorber les filtres dans la blanc préparé.
-
Filtration
Filtrer les solutions avant analyses
Étape de préparation N°3
-
Solvant ou solution
- SOLUTION BLANC FILTRE
-
Type de préparation
Désorption -
Volume
5 mL -
Autres conditions de préparation
Préparer un volume de blanc filtre en plaçant n filtres imprégnés vierges dans n x 20 mL d’eau.
Refermer la cassette et replacer le bouchon inférieur.
Introduire 5 mL de blanc filtre par l’orifice supérieur de la cassette et agiter manuellement.
-
Filtration
Filtrer les solutions avant analyses
Commentaires, conseils, conditions particulières
Traiter les blancs de laboratoire et blancs de terrain de la même manière que les échantillons prélevés.
Toutes les solutions sont filtrées avant dosage chromatographique.
Une condition analytique :
Condition analytique N°1
-
Technique analytique
- CHROMATOGRAPHIE IONIQUE AVEC MEMBRANE DE SUPPRESSION
-
Injecteur
- PASSEUR AUTOMATIQUE
-
Colonne
- ECHANGEUSE D'IONS
- SUPRESSEUR
-
Détecteur
- CONDUCTIMETRIE
Étalonnage et expression des résultats
La méthode d'étalonnage indiquée est celle utilisée lors du développement. Elle n'a cependant pas de caractère obligatoire
-
Principe d'étalonnage
externe -
Solvant de l’étalon
- Même solvant que celui des échantillons
-
Commentaires
Étalonnage
- Préparer une gamme d'étalonnage, en général de 0,2 à 10 mg/L en NH4+ à partir de substances de référence,commerciales ou synthétisées en laboratoire.
- Introduire un filtre en fibre de quartz imprégné dans chaque flacon.
- Une gamme d'étalonnage comprendra un minimum de 5 points.
- Analyser les étalons.
- Tracer la courbe d'étalonnage (polynôme de second degré - voir données de validation).
Dosage
Filtrer les solutions de désorption (filtres prélevés, blancs de laboratoire et blancs de terrain) et les injecter suivant les mêmes conditions analytiques.
Diluer si nécessaire les échantillons dans le blanc filtre de façon à rester dans la gamme d'étalonnage.
-
Calcul de la quantité de substance sur le dispositif
Cas des membranes ou filtres en fibre de quartz non imprégnés et parois de la cassette
La concentration des échantillons (en mg/L) est déterminée sur la courbe d’étalonnage.
Les cations NH4+ recueillis sur le filtre non imprégné et les parois de la cassette sont d'origine particulaire, le résultat est exprimé en mg/m3 de NH4+ particulaire.
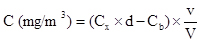
avec :
Cx (mg/L) : sommes des concentrations de l’ion NH4+ dans les échantillons (filtres non imprégnés et cassettes)
d : facteur de dilution
Cb (mg/L) : moyenne des concentrations de l’ion NH4+ dans les blancs de laboratoire
v (mL) : volume de reprise des échantillons (5 mL de blanc filtre imprégné)
V (L) : volume d’air prélevé
Cas des filtres imprégnés
La concentration des échantillons est déterminée sur la courbe d’étalonnage.
La concentration du polluant P (ici NH3) dans l’atmosphère est donnée par :
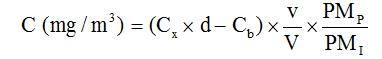
avec :
Cx (mg/L) : concentration de l’ion NH4+ dans l’échantillon
d : facteur de dilution
Cb (mg/L) : moyenne des concentrations de l’ion NH4+ dans les blancs de laboratoire
v (mL) : volume de reprise des échantillons (20 mL d’eau)
PMP : poids moléculaire du polluant NH3 (17 g/mol)
PMI : poids moléculaire de l’ion NH4+ (18 g/mol)
V (L) : volume d’air prélevé
Compléments
Phase mobile à déterminer en foction de la colonne utilisée. Des exemples sont donnés dans les données de validation.
Interférences
Une forte concentration en sodium peut gêner les dosages de NH4+. Dans ce cas et selon la colonne utilisée, il est conseillé d’utiliser un éluant qui retarde les temps de rétention des pics du sodium et de NH4+, et permet une meilleure séparation de ces 2 pics (voir exemples de chromatogramme dans les données de validation - compléments).
Autres méthodes utilisables
Chromatographie ionique sans suppression, détection conductimétrique.
Electrophorèse capillaire.
Electrode spécifique NH3 à diffusion gazeuse.
Bibliographie
- NF EN 1076 – Exposition sur les lieux de travail. Procédures pour le mesurage des gaz et vapeurs à l’aide de dispositifs de prélèvement par pompage. Paris, Association française de normalisation (AFNOR), 2010, 36 p.
- NF EN 482 – Exposition sur les lieux de travail. Exigences générales concernant les performances des procédures de mesure des agents chimiques. La Plaine Saint Denis, Association française de normalisation (AFNOR), 2012, 18 p.
Historique
| Version | Date | Modification(s) faisant l’objet de la nouvelle version |
|---|---|---|
| 013/V01 |
| Création et mises à jour |
| 013/V01 | 31/03/2008 | Nouvelle présentation. Imprégnation du filtre de quartz (pour l’ammoniac) dans la cassette de prélèvement. Création de l’historique. |
| 013/V02 | 15/12/2014 | Corrections dans la fiche suite à nouvelle mise au point et ajout des données de validation Annexe 2 Corrections glossaire |
| M-13/V01 | Novembre 2015 | Mise en ligne Prélèvement sur cassette fermée Substances : ammoniac et sels d'ammonium Analyse par chromatographie ionique |
| M-13/V02 | Octobre 2020 | Correction temps de prélèvement 4 h à 2 L/min 8 h à 1 L/min Ajout données de validation - essai de claquage à 1 L/min |
Date de mise à jour : octobre 2020
Ancien numéro de fiche MétroPol : 013
