Pathologie - Toxicologie
-
Toxicocinétique - Métabolisme [1]
L’aniline pénètre dans l’organisme par toutes les voies d’exposition ; elle se distribue largement dans les tissus et est métabolisée dans le foie et éliminée majoritairement dans les urines sous forme de métabolites ou sous forme libre.
Chez l'animal
Absorption
L'aniline est un composé liposoluble qui est facilement absorbé par inhalation, par ingestion et à travers la peau. Le taux d'absorption par voie orale est de 89 - 96 % de la dose chez le rat et de 72 % chez la souris.
Distribution
Après absorption, l'aniline se distribue dans tout l'organisme ; chez le rat, la plus forte concentration est retrouvée dans les globules rouges puis le plasma, la rate, les reins, le foie, les poumons, le cœur, le cerveau et le tissu adipeux [12]. Le pic plasmatique apparaît, chez le rat, 0,5, 1 ou 2 heures après l’administration d’une dose unique de 10, 30 ou 100 mg/kg d’aniline respectivement [12]. Après 24 heures, la concentration d'aniline diminue à moins de 2 % de la valeur du pic dans le plasma mais demeure élevée dans les organes (reins > foie > poumons, cœur, rate, cerveau). Après 48 heures, il reste dans les tissus moins de 0,1 % de la dose administrée.
Chez le rat, l’administration répétée par voie orale de 14C-aniline pendant 10 jours induit une accumulation des molécules radiomarquées fixées de façon covalente dans les globules rouges et la rate [12]. La fixation de l'aniline aux macromolécules, notamment pour former des adduits avec l'hémoglobine, est plus faible chez la souris que chez le rat.
L’aniline traverse la barrière placentaire facilement [13].
Métabolisme
L'aniline est métabolisée dans le foie selon la figure 1.
Schéma métabolique
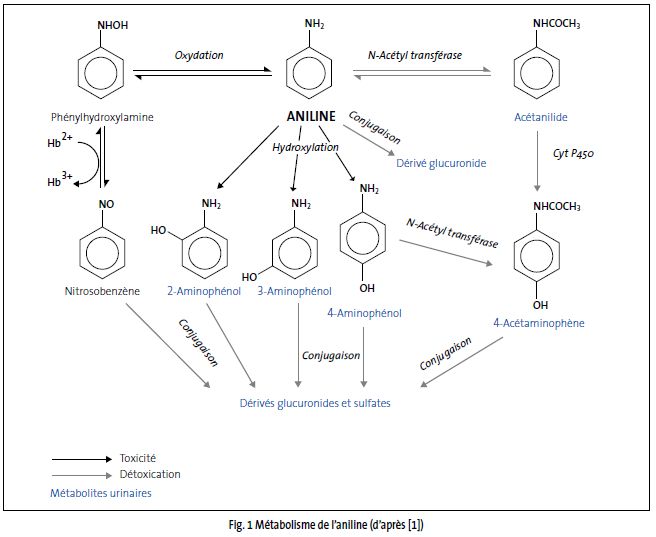
Excrétion
Dans l'organisme, trois voies métaboliques existent et aboutissent à la formation de conjugués, éliminés majoritairement dans les urines :
- une N-hydroxylation (voie de bioactivation) qui donne naissance à de la phénylhydroxylamine dont une partie se transforme en nitrosobenzène (réaction réversible). Ces deux métabolites ont été mis en évidence dans le sang de rats traités, mais pas dans leurs urines ;
- une N-acétylation via la N-acétyltransférase (voie de détoxication) qui engendre la formation d’acétanilide et de 4-acétaminophène ;
- une hydroxylation du noyau aromatique qui aboutit à la formation de 2-, 3- et 4-aminophénol. Le pourcentage relatif de ces isomères et de leurs dérivés conjugués varie selon l'espèce animale considérée.
Les animaux excrètent, en 3 jours, entre 70 et 89 % de la dose orale dans les urines, en majorité sous forme de dérivés N-acétylés de l'aniline.
Chez le rat, le métabolite majeur à faible dose (< 50 mg/kg par voie orale) est l'acétaminophène sulfo-conjugué ; au-delà de cette dose, une saturation de la voie métabolique (via la N-acétyltransférase) est observée, conduisant à l'élimination de 4-aminophényl-sulfate et de N-acétyl-4-aminophénylglucuronide. Chez la souris, les dérivés glucurono-conjugués représentent la majorité des métabolites excrétés ; il n'y a pas de saturation de cette voie métabolique.
Le rapport des 4-aminophénol et 2-aminophénol éliminés dans l'urine est variable selon les espèces : il est égal à 11 chez le cobaye, 6 chez le lapin et le rat mâle, 2,5 chez le rat femelle, 1,6 chez la souris et 0,5 chez le chat et le chien.
Chez l'Homme
L'aniline est bien absorbée, de façon prépondérante par voie pulmonaire (environ 90 % de la quantité inhalée) et par voie cutanée, mais aussi par voie digestive [14]. L'absorption percutanée peut atteindre 38 % de la dose appliquée et la vitesse d'absorption à 0,18 - 0,72 mg/cm²/h pour la forme liquide. Sous forme vapeur (5 – 30 mg/m3), l'aniline pénètre à travers la peau 1000 fois moins rapidement (environ 0,2 à 0,4 µg/cm²/h) ; cependant, à concentrations plus faibles, l'absorption cutanée est plus importante que l'absorption respiratoire (surtout en présence de forte chaleur et d'humidité).
L'aniline est métabolisée dans le foie (de façon identique au métabolisme animal) et éliminée dans les urines sous forme de 4-acétaminophène (ou paracétamol, entre 56 et 69 % de la dose orale administrée), de métabolites conjugués (N-acétyl-4-aminophénylglucuronide, entre 2,5 et 6,1 %), d’acétanilide et d’aniline inchangée [15]. Seule une faible fraction (< 0,4 %) de la quantité absorbée est éliminée sous forme inchangée dans les urines et l'air expiré [14].
Les demi-vies de ces métabolites sont comprises entre 1 et quelques heures [13].
Surveillance Biologique de l'exposition
L’absorption cutanée de l’aniline pouvant être significative, la surveillance biologique est particulièrement intéressante pour apprécier l'intensité de l'exposition.
Le dosage de l'aniline (avec hydrolyse acide) dans les urines en fin d’exposition ou fin de poste est à privilégier pour la surveillance biologique des travailleurs exposés.
Les valeurs biologiques d’interprétation (VBI) professionnelles proposées sont basées sur la relation avec la méthémoglobinémie (méthémoglobinémie attendue inférieure à 5 %, considérée comme ne présentant pas de risque pour la santé). Une VBI issue de la population générale, basée sur le 95ème percentile des valeurs chez des sujets non-fumeurs, est également disponible.
Le taux de méthémoglobine est un indicateur d'effet biologique ayant été proposé pour la surveillance biologique de l’exposition à des agents méthémoglobinisants. C’est un indicateur non spécifique et non quantitatif. Il a également l’inconvénient de nécessiter un prélèvent immédiatement en fin de poste et une analyse dans l'heure suivant le prélèvement en raison de son instabilité. Une méthémoglobinémie supérieure à 1,5 % suggère une exposition à un agent méthémoglobinisant. Des VBI professionnelle et issue de la population générale sont disponibles pour cet indicateur.
-
Mode d'actions
L'exposition à l'aniline engendre la formation de méthémoglobine. Chez le chien, une exposition orale unique induit jusqu'à six fois plus de méthémoglobine qu'une exposition par inhalation à concentration comparable.
La phénylhydroxylamine et le nitrosobenzène jouent un rôle majeur dans le mécanisme d'action toxique de l'aniline. La méthémoglobine est formée dans l'organisme par oxydation du fer ferreux (Fe2+) de l'hémoglobine en fer ferrique (Fe3+) ; elle est incapable de fixer l'oxygène et donc de le transporter. Habituellement, elle n'excède pas 2 % de l'hémoglobine totale et est rapidement réduite par un système enzymatique : la méthémoglobine-réductase. L'intoxication par l'aniline provoque une méthémoglobinémie importante qui résulte du débordement des capacités de réduction du système enzymatique par la présence de la phénylhydroxylamine et du nitrosobenzène.
Chez l’Homme, l'activité de l'enzyme N-acétyltransférase est modulée génétiquement, séparant la population en « acétylateurs rapides » et « acétylateurs lents » ; ces derniers forment plus de phénylhydroxylamine, nitrobenzène et 4-aminophénol que d'acétanilide et de ce fait plus de méthémoglobine [1].
-
Toxicité expérimentale
Toxicité aiguë
L’aniline est nocive pour les animaux, après exposition orale, cutanée ou inhalatoire, par son action méthémoglobinémiante. Elle est sensibilisante et irritante pour la peau et les yeux.
Chez le rat, la DL50 par voie orale est comprise entre 442 mg/kg et 780 mg/kg (femelles) ou 930 mg/kg (mâles) ; la CL50 par inhalation, chez le rat, varie selon le mode d'exposition : tête seule 839 ppm (3,3 mg/L)/4 h, corps entier 478 ppm (1,9 mg/L)/4 h ; la DL50 par voie cutanée est de 1540 mg/kg chez le lapin et, de façon surprenante, de 1290 mg/kg (peau intacte) ou 2150 mg/kg (peau abrasée) chez le cobaye. La sensibilité de la souris et celle du chien semblent assez proches de celle du rat. Le chat est nettement plus sensible (DL50 cutanée : 254 mg/kg, létalité par voie orale : 50 - 100 mg/kg).
Pour toutes ces espèces, les manifestations observées (tremblements, cyanose, hyperpnée, convulsions, hypersalivation, prostration) résultent de la toxicité hématologique de l'aniline se traduisant par une méthémoglobinémie et une hémolyse. La dose sans effet méthémoglobinémiant chez le rat est de 20 mg/kg par voie orale.
Localement, chez le lapin, l'application cutanée de 0,5 mL d'aniline pure sous pansement occlusif produit une irritation modérée (érythème) réversible en 8 jours ; cependant, lors d'expositions cutanées à doses sublétales, les animaux présentent des hémorragies sous-dermiques et un érythème sévère. L'instillation de 50 mg d'aniline pure dans l'œil du lapin provoque une irritation sévère avec opacité cornéenne et érythème conjonctival, non réversible en 8 jours.
L'aniline est sensibilisante pour le cobaye aux concentrations d'induction de 1,5 % et de déclenchement de 20 %.
Toxicité subchronique, chronique [12]
Le principal effet de l’aniline en exposition répétée ou prolongée est hématologique (lésion des érythrocytes, anémie hémolytique, méthémoglobinémie, augmentation des corps de Heinz).
Chez le rat, par voie orale (≥ 7mg/kg pc/j d'aniline, pendant 2 ans) ou inhalatoire (≥ 5 ppm, pendant 26 sem, 5 j/sem, 6 h/j), on observe des modifications du système hématopoïétique avec des lésions correspondantes de la rate (augmentation de poids, congestion vasculaire, dépôt d'hémosidérine, hyperplasie et fibrose du stroma), de la moelle osseuse (hyperplasie érythroïde), des reins (hémosidérose tubulaire) et du foie (augmentation de poids et hémosidérose). Les signes cliniques sont : cyanose, baisse de la prise de poids et de nourriture, et létalité à fortes doses. Aucune NOAEL par voie orale n'a pu être établie ; la LOAEL est de 7 mg/kg pc/j.
Un effet toxique similaire a été obtenu après exposition par inhalation ; une NOAEC de 32,4 mg/m3 (6 h/j, 2 sem) a été établie pour les effets sur le système hématopoïétique [16].
Chez la souris, on observe une atteinte hépatique (inflammation du canal biliaire, ≥ 0,6 % dans la nourriture soit environ 730 mg/kg pc/j) et une baisse de la prise de poids (1,2 % dans la nourriture soit environ 1500 mg/kg pc/j) ; cependant, au cours de cette étude, les paramètres hématologiques n'ont pas été évalués.
Effets génotoxiques [13]
Aussi bien in vitro que in vivo, l’aniline est à l’origine de nombreux dommages à l’ADN, sur des cellules humaines et non humaines (essentiellement aberrations chromosomiques, micronoyaux et échanges entre chromatides sœurs).
De nombreuses études sont disponibles in vitro et in vivo, sur cellules humaines et sur cellules de rongeurs, mettant en évidence les propriétés génotoxiques de l’aniline (cf. tableau 2 ci-dessous).
Test
Cellules / animal
Activation métabolique
Résultat
In vitro
Test d’Ames
S. typhimurium TA98, TA100, TA1535 et TA1537
+/-
Négatif
Mutation génique
Cellules de lymphome de souris
+/-
Positif
Aberrations chromosomiques
Cellules ovariennes de hamster chinois (CHO)
+
Positif (forte dose)
-
Résultats variables
Micronoyaux
Cellules embryonnaires de hamster syrien
-
Négatif
Cellules pulmonaires de hamster chinois
-
Négatif
+
Positif
Echanges de chromatides sœurs
Fibroblastes humains
+/-
Positif
Cellules épithéliales de foie de rats
-
Positif
CHO
+/-
Positif (forte dose)
Cassures de l’ADN
Cellules de lymphome de souris
+
Positif (forte dose)
Cellules pulmonaires de hamster chinois
-
Négatif
Cellules humaines
-
Positif
In vivo
Micronoyaux / moelle osseuse
Rat, voie orale (eau de boisson)
Positif (à partir 287 mg/kg pc, une dose)
Souris, voie orale
Positif (2 doses de 23 mg/kg pc, souris B6C3F1)
Négatif (1 dose de 250 mg/kg pc, souris ICR)
Souris, intra-péritonéale (ip)
Résultats variables selon les souches de souris et le nombre d’injections
Micronoyaux / sang périphérique
Rat, voie orale, gavage 28 jours
Positif (100 mg/kg pc/j)
Souris, voie orale (nourriture), 90 jours
Positif (à partir de 65 mg/kg pc/j)
Aberrations chromosomiques / moelle osseuse
Souris, ip
Négatif (380 mg/kg pc, 2 doses)
Rats, voie orale
Positif (500 mg/kg pc, 1 dose)
Cassures de l’ADN / test d’élution alcaline
Rats, ip
Positif dans le foie (105 et 210 mg/kg pc)
Positif dans les reins (210 mg/kg pc)
Souris, ip
Positif dans les reins (300 mg/kg pc)
Négatif dans le foie (300 et 420 mg/kg pc) et la moelle osseuse (420 mg/kg pc)
Cassures de l’ADN / test des comètes
Rats, voie orale, 150 mg/kg pc
Positif dans la vessie, les poumons, le foie, les reins, le côlon et l’estomac (à différents temps)
Négatif dans le cerveau et la moelle osseuse
Souris, voie orale, 100 ou 1000 mg/kg pc
Positif dans la vessie, les poumons, le foie, le colon, le cerveau et la moelle osseuse (à différents temps)
Négatif dans l’estomac et les reins
Tableau 2 : Principaux résultats obtenus dans les tests de génotoxicité réalisés in vitro et in vivo concernant l’aniline [13].
Par ailleurs, l’aniline est à l’origine de stress oxydatif caractérisé notamment par :
- une augmentation de la 8-hydroxy-2’-désoxyguanosine (considéré comme un biomarqueur des dommages oxydatifs de l’ADN),
- une augmentation dose dépendante des espèces réactives de l’oxygène et de l’azote, et des niveaux de malondialdéhyde, et
- une déplétion en glutathion.
Effets cancérogènes [13]
L’aniline est cancérogène pour le rat, induisant des carcinomes spléniques surtout chez les mâles, mais pas pour la souris.
Les tests de transformation cellulaire in vitro donnent des résultats positifs ou négatifs, selon les modèles cellulaires utilisés.
Selon les récentes conclusions du CIRC, il existe des preuves suffisantes de cancérogénicité chez les animaux de laboratoire, basée sur l’augmentation de l’incidence des néoplasmes malins (dans 2 études indépendantes sur une espèce, le rat). De plus, il existe des preuves solides que l'aniline présente les caractéristiques « clés » des cancérogènes dans les systèmes expérimentaux : activation métabolique en molécules électrophiles, génotoxicité, induction de stress oxydatif et altération de la prolifération cellulaire, la mort cellulaire ou l'apport en nutriments. Le CIRC l’a classée dans le groupe 2A, substance probablement cancérogène pour l’Homme.
In vivo, chez le rat, l'aniline administrée sous forme de chlorhydrate dans la nourriture (10 - 30 - 100 mg/kg pc/j soit 7 - 22 - 72 mg d'aniline/kg pc/j, 104 sem) provoque des tumeurs de la rate chez les mâles uniquement, dont la majorité sont des sarcomes, des hémangiosarcomes et/ou des fibrosarcomes. Au niveau des testicules, l’incidence des mésothéliomes de la tunique vaginale tend à augmenter (avec augmentation statistiquement significative à la dose intermédiaire). À des doses plus fortes (174,4 et 360,5 mg/kg/j dans la nourriture), apparaissent en plus des tumeurs de la rate précédemment citées, chez les mâles à toutes les doses et chez les femelles à la plus forte dose, des tumeurs du mésenchyme (hémangiosarcome, fibrosarcome et sarcome) dans les organes des cavités pleurale et abdominale.
Les souris mâles et femelles exposées à l'aniline sous forme de chlorhydrate dans la nourriture (0 - 0,6 - 1,2 % soit environ 0 - 735 - 1550 mg/kg/j, 103 sem), ne développent aucune tumeur.
La différence de toxicité entre le rat et la souris pourrait être expliquée par une différence de métabolisme. Chez la souris, la voie de métabolisation et d'excrétion de l'aniline n'est pas saturable contrairement au rat. Des études de cancérogenèse effectuées sur les principaux métabolites de l'aniline (p- ou o-aminophénol, phénylhydroxylamine, nitrosobenzène) se sont révélées négatives.
Effets sur la reproduction [12]
L’aniline n’agit pas sur les organes reproducteurs des animaux ni sur le développement des petits, même à une dose toxique pour les mères.
Fertilité
Il n'y a pas d'étude spécifique de l'effet de l'aniline sur la fertilité des animaux. Cependant, lors des études en exposition à long terme, aucun effet n'a été noté sur les organes reproducteurs du rat ou de la souris.
Développement
L'aniline n'agit pas sur le développement pré- ou post-natal du rat à des doses qui induisent une toxicité hématologique chez les mères (gavage, 0-7-22-72 mg/kg pc/j d’aniline, du 7ème au 20ème jour de gestation). Elle n'induit qu'une légère augmentation de poids du foie fœtal à la forte dose sans effet hématologique en dehors d'une faible augmentation de taille des globules rouges, qui persiste après la naissance. Aucune NOAEL pour la toxicité maternelle n'a pu être établie ; la NOAEL pour le développement est 30 mg de chlorhydrate d'aniline, correspondant à 22 mg d'aniline/kg pc/j.
-
Toxicité sur l’Homme
Les intoxications aiguës qui surviennent essentiellement par contact cutané ou ingestion se traduisent par une méthémoglobinémie et une hémolyse avec des complications cardiovasculaire, hépatique et rénale. En cas d'exposition chronique, on peut noter des signes discrets d'atteinte neurologique, de cyanose et d'anémie hémolytique. Les cancers vésicaux, initialement attribués à l'aniline dans des études anciennes, semblent en fait en lien avec d'autres amines aromatiques cancérogènes. Les données sont insuffisantes pour juger des effets sur la fonction de reproduction chez l'Homme.
Toxicité aiguë [1]
Les effets de l'intoxication aiguë par l'aniline résultent de la formation accrue et rapide de méthémoglobine, à l'origine d'une anoxie. La cyanose «bleu-ardoisée», signe majeur et le plus précoce, prédominant à la face et aux extrémités, apparaît lorsque 10 à 15 % d'hémoglobine ont été oxydés (soit environ 1,5 g de méthémoglobine pour 100 mL de sang). Lorsque le rapport méthémoglobine/hémoglobine dépasse 30 % (soit environ 5 g de méthémoglobine pour 100 mL de sang), la cyanose devient plus intense et s'accompagne de signes fonctionnels : dyspnée, tachycardie, vomissements, céphalées, angoisse, agitation précédant des troubles de conscience (somnolence, voire coma). À ce stade, la méthémoglobinémie est souvent associée à une hémolyse responsable d'une anémie et d'une hémoglobinurie, et pouvant se compliquer d'une insuffisance circulatoire aiguë et d'une insuffisance rénale aiguë par néphropathie tubulo-interstitielle. Un ictère hépatique résulte parfois de l'anémie hémolytique, et des évolutions mortelles ont été signalées lorsque le rapport méthémoglobine/hémoglobine atteint 60 à 65 %, ou en raison des complications de l'intoxication. Dans certains cas mortels, des altérations dégénératives des reins, du foie, du cœur, ainsi qu'un œdème cérébral et pulmonaire ont été rapportés.
Des manifestations discrètes peuvent se rencontrer pour des expositions de quelques heures à des concentrations atmosphériques comprises entre 7 et 53 ppm d'aniline, et des signes d'intoxication plus sévères sont observés après 1 heure d'exposition à des concentrations comprises entre 105 et 160 ppm. La plupart des accidents aigus chez l'Homme proviennent toutefois de la pénétration du produit à travers la peau (directement ou à travers les vêtements) ou de l'ingestion accidentelle, même de faibles doses. L'absorption d'éthanol est un facteur aggravant de l'intoxication, notamment du risque hémolytique.
On ne dispose pas de données suffisantes pour juger d'un risque d'irritation cutanée ou respiratoire chez l'Homme. L'exposition à des vapeurs d'aniline a provoqué une irritation oculaire associée à une photophobie et une atteinte visuelle. Ces perturbations conjonctivales et cornéennes sont transitoires et observées avec d'autres amines [17].
Toxicité chronique [1]
Des intoxications chroniques peuvent survenir à la suite d'expositions répétées à de faibles concentrations de produit. Elles se manifestent par l'apparition de céphalées, vertiges, asthénie et d'une cyanose discrète qui régresse rapidement après la fin de l'exposition. Des anémies hémolytiques généralement modérées ont été signalées, avec un processus de régénération marqué par la présence de nombreux réticulocytes circulants.
Des réactions positives à des patchs cutanés à l'aniline sont retrouvées chez des sujets présentant une dermatose de contact. Il n'est toutefois pas possible d'affirmer que l'aniline soit la cause de l'allergie, une réaction croisée avec certaines substances ayant un groupe aminé en -para est en effet retrouvée.
Effets cancérogènes [18, 19]
Le risque élevé de cancer vésical observé dans la première moitié du XXième siècle chez les travailleurs de l'industrie des colorants à base d'aniline peut, en fait, être attribué à l'exposition à des produits autres que l'aniline, reconnus aujourd'hui comme cancérogènes pour l'Homme : benzidine et 2-naphtylamine. En effet, des études épidémiologiques portant sur des travailleurs exposés à l'aniline, mais pas à ces cancérogènes reconnus, n'ont pas montré d'augmentation significative de la fréquence des décès dus à des cancers :
- cancer de la vessie observé dans une cohorte de 1 233 travailleurs, fabriquant ou utilisant de l'aniline, contre 0,83 attendu d'après les résultats de mortalité de la population générale [20] ;
- aucun cancer de la vessie observé chez 342 travailleurs employés à la fabrication de colorants synthétiques selon 3 procédés, dont 2 faisaient appel à de l'aniline comme matière première[21].
Par contre, dans une étude plus récente[22], un excès de tumeurs de la vessie est observé chez des salariés exposés à de l'o-toluidine et de l'aniline (ainsi qu'à d'autres substances non prises en compte). Sur 708 sujets exposés à ces 2 substances, 7 cas de cancers de la vessie ont été observés (1,08 attendu, taux d'incidence relative 6,48 [3,04 - 12,2]) ; les auteurs montrent chez les exposés une augmentation des adduits spécifiques à l'aniline et à l'o-toluidine. Ils concluent que l'action cancérogène de l'o-toluidine est vraisemblable mais qu'un effet de l'aniline ne peut être totalement exclu [23].
Effets sur la reproduction
Il n'existe pas de données suffisantes chez l'Homme pour évaluer la toxicité de l'aniline sur la fertilité ou le développement.
-
Interférences métaboliques
-
Cohérence des réponses biologiques chez l'homme et l'animal
